IVD-Kits bestehen aus einer Kombination von zum Teil proteinhaltigen Reagenzien. In Kombination mit entsprechenden Analysegeräten des Anbieters ist es möglich, eine große Anzahl von Proben weitgehend automatisiert zu untersuchen. In der EU werden IVDs über die Verordnung 2017/746 geregelt, und die Hersteller müssen zum Nachweis der Konformität als Medizinprodukt aufwendige Validierungsstudien durchführen.
In der IVD spielen nicht-ionische Tenside, die unspezifische Bindungen zwischen Proteinen verhindern und wässrige Lösungen stabilisieren, eine wichtige Rolle. Etabliert habe sich u. A. Nonylphenol-ethoxylate (abgekürzt NPE oder NPEO) und insbesondere Octylphenolethoxylate (abgekürzt OPE oder OPEO). Sie werden sowohl für die Gewinnung von Proteinen als auch als Bestandteil von IVD-Reagenzien eingesetzt.
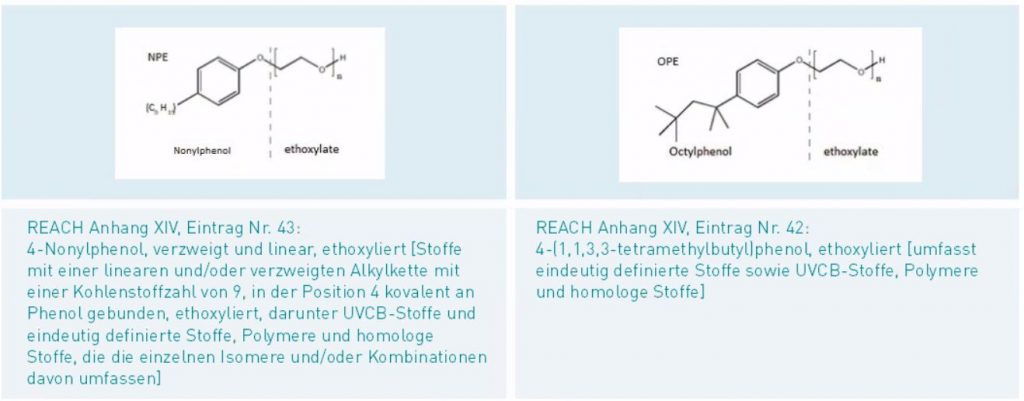
Chemisch handelt es sich um alkylierte Phenolderivate, die an der Hydroxyl-Gruppe mit einer Polyethylenglykolkette (siehe Strukturformeln auf der nächsten Seite) verbunden sind. Die Stoffbezeichnungen umfassen jeweils eine Gruppe von Verbindungen mit unterschiedlicher Länge der Polymerkette. Auch der Verzweigungsgrad der Alkylkette kann variieren. NPE und OPE waren bisher sehr verbreitet verwendete Tenside in der chemischen Industrie, der Pharmaindustrie und in Laboranwendungen. Bei der bekannten Laborchemikalie Triton™ X‑100 zum Beispiel handelt es sich um 4-(1,1,3,3‑tetramethylbutyl)phenol, ethoxyliert mit durchschnittlich n=9,5 Ethylenglykol-Einheiten.
Endokrinschädliche Eigenschaften führen zur Aufnahme in die REACH Kandidatenliste
Alkylphenolethoxylate werden in Kläranlagen und in der Umwelt biologisch abgebaut, wobei die Polymerketten schrittweise verkürzt werden. Übrig bleiben relativ schwer abbaubare Alkylphenole. Die Abbauprodukte Nonylphenol (NP) bzw. Octylphenol (OP) gelten aufgrund ihrer hormonellen Wirkung auf Wasserorganismen als so genannte „endocrine disruptors“.
Auch wenn NPE und OPE diese Eigenschaft selbst nicht haben, setzten sie letztlich endokrinschädliche Stoffe frei und werden daher inzwischen als ebenso umweltgefährlich angesehen wie ihre freien Alkylphenole. Daher wurden nicht nur NP und OP sondern auch NPE und OPE mit Verweis auf REACH Artikel 57(f) (siehe ganz unten) in die Liste der für eine Zulassung in Frage kommenden besonders besorgniserregenden Stoffe (SVHC1) – der REACH-Kandidatenliste – aufgenommen.
Zulassungspflicht für NPE und OPE
NPE ist in vielen Anwendungen verboten wie zum Beispiel in Reinigungsmitteln, in der Textil- und Lederverarbeitung, in der Metallverarbeitung und Papierherstellung. Die in der EU verwendete Menge ist aber weiterhin hoch. Auch OPE wird in großen Mengen in der EU eingesetzt und war bisher nicht beschränkt. Angesichts der großen Mengen und der endokrinschädlichen Eigenschaften der Abbauprodukte wurden daher beide Stoffe 2017 in den Anhang XIV der REACH-Verordnung aufgenommen. NPE mit dem Eintrag Nr. 43 und OPE mit dem Eintrag Nr. 42.
Das bedeutet, dass die weitere Verwendung der Stoffe nach einem im Anhang angegebenen Ablaufdatum verboten ist, es sei denn, für die jeweilige Verwendung wurde eine Zulassung beantragt. Bei NPE und OPE ist das Ablaufdatum der 4. Januar 2021, der Antrag musste ggf. bis zum 4. Juli 2019 eingereicht werden.
Die Aufnahme in den Anhang XIV kommt für viele Anwender einem Verbot des Stoffes gleich, denn die Antragstellung ist sehr aufwendig und langwierig und damit auch teuer. Eine Zulassung durch die Kommission wird nur gewährt, wenn der Antragsteller zeigen kann, dass entweder die Risiken der weiteren Verwendung angemessen beherrscht werden oder, dass der sozio-ökonomische Nutzen der Verwendung die Risiken überwiegt. Das Ziel ist es aber letztlich diese Stoffe wo möglich zu substituieren.
Dies betrifft auch die Verwendung von NPE und OPE in der In-Vitro-Diagnostik. Es gibt eine vieldiskutierte Ausnahme von der Zulassung für wissenschaftliche Forschung und Entwicklung, die ausdrücklich auch auf IVD angewendet werden kann (siehe Q&A 1442 der ECHA). Viele Anbieter von IVD-Kits kamen jedoch zu dem Schluss, dass diese Ausnahme auf ihre Produkte nicht oder nur teilweise anwendbar ist, weil sie voraussetzt, dass die Verwendung unter kontrollierten Bedingungen erfolgt. Kontrollierte Bedingungen sind aber nur dann erfüllt, wenn die umweltgefährlichen Alkylphenole nicht in die Umwelt freigesetzt werden können. Dazu müssten die NPE- bzw. OPE-haltigen Lösungen nach der Analyse gesammelt und entsorgt werden. Tatsächlich ist es aber in Laboren europaweit durchaus üblich und in Einklang mit den lokalen Abwasservorschriften, dass die stark verdünnten Lösungen nach der Analyse in das kommunale Abwasser entlassen werden. Dort werden die Ethoxylate abgebaut und die relativ stabilen Alkylphenole dann in Flüsse und Meere weiter transportiert. Welcher Anteil der Lösungen in das Abwasser gelangt, ist in der Regel nicht bekannt.
Zulassungsanträge für IVD
Da die meisten Labore, die NPE- oder OPE-haltige IVD-Kits verwenden, mit der Beantragung der Zulassung überfordert wären, haben sich viele Hersteller entschieden, entsprechende Anträge, die die Endanwendung abdecken, auszuarbeiten und bei der ECHA einzureichen2. Hierbei ergeben sich für die Antragsteller insbesondere folgende Herausforderungen:
- Die emittierten Lösungen sind zwar extrem verdünnt, für die beobachteten endokrinen Effekte kann aber kein sicherer Konzentrationswert abgeleitet werden (der sogenannte PNEC3). Ein Risiko für die Umwelt kann daher trotzdem nicht ausgeschlossen werden;
- Wenn die Menge an tatsächlich emittierten Tensiden nicht bekannt ist, muss der Hersteller davon ausgehen, dass 100% der in IVD-Kits eingesetzten Menge in die Umwelt gelangt (worst case scenario);
- Zwar gibt es diverse alternative Tenside, die keine vergleichbare Problematik aufweisen, die Hersteller dürfen aber die Stoffe nicht einfach ersetzen. Die Registrierung als Medizinprodukt ist spezifisch für die jeweilige Zusammensetzung, eine Änderung kann die Funktionalität und Zuverlässigkeit der Tests beeinträchtigen. Wenn ein Anbieter sein betreffendes Analysesystem also nicht einstellen will, muss er die Stoffe mindestens so lange weiterverwenden, bis er ein neu entwickeltes alternatives Produkt registriert hat. Auch die Laufzeiten der Analysegeräte sind relevant. Ein neues Produkt für eine alte Plattform aufwendig zu validieren ist wirtschaftlich unsinnig.
Da die Risiken für die Umwelt wie oben beschrieben nicht angemessen beherrscht werden können, mussten die Antragsteller im Rahmen einer sozio-ökonomischen Analyse zeigen, dass der Nutzen durch die weitere Verwendung die Risiken aufwiegt. Dies beinhaltet sowohl Nutzen der Diagnostik für die Gesellschaft als auch die mit der Herstellung und Vermarktung verbundenen Arbeitsplätze und wirtschaftlichen Aspekte für die betroffenen Unternehmen. Anhand eines Substitutionsplans mussten die Antragsteller erklären, was sie dafür tun, die zulassungspflichtigen Stoffe zu ersetzen und bis wann. Bei den meisten Antragstellern ist eine schrittweise Substitution über 2 bis 12 Jahre vorgesehen.
Bewertung der Zulassungsanträge durch Fachgremien
Eingereichte Zulassungsanträge werden durch zwei Fachgremien der ECHA bewertet: den Ausschuss für Risikobewertung – RAC (Risk Assessment Committee) und den Ausschuss für Sozio-ökonomische Analyse – SEAC (Committee for Socio Economic Analysis). Deren Standpunkte („opinions“) werden auf der Seite der ECHA veröffentlicht und sind die Grundlage für die Entscheidung der EU-Kommission im Ausschussverfahren.
Standpunkte der Fachgremien liegen inzwischen für viele der Anträge für NPE oder OPE in IVD-Anwendungen vor, weitere befinden sich noch in der Prüfung. Dabei zeichnet sich ab, dass RAC und SEAC zwar die Zulassung generell unterstützen, der RAC jedoch angesichts der verbleibenden Risiken für die Umwelt in vielen Anträgen dies nur unter zusätzlichen Auflagen empfiehlt. Diese betreffen die Sammlung und Entsorgung NPE- bzw. OPE-haltiger Abwässer und deren separate Entsorgung, um die Emissionen in die Umwelt zu verringern. Entschieden wurde Stand November 2020 noch über keinen dieser Anträge.
Aufwendige Abwassertrennung für Krankenhäuser und Labore?
Der RAC fordert zwar keine bestimmte Maßnahme zur Minimierung der Umwelteinträge, das einzig verlässliche und halbwegs praktikable Verfahren ist aber, die NPE/OPE-haltigen Abwässer als gefährlichen Abfall zur Verbrennung zu entsorgen. Bei der Verbrennung werden die Stoffe nachweislich zerstört.
Dies erscheint bei Verbräuchen von wenigen Millilitern Lösung pro Test zumutbar, jedoch ist zu bedenken, dass auf einem Analysesystem täglich eine große Anzahl Tests in der Regel unter Einsatz mehrere IVD-Kits im Wechsel durchgeführt werden, und nur ein Teil davon enthält NPE oder OPE. Da in diesem Fall sämtliche Abwässer gesammelt werden müssen, kann sich die tägliche Menge an Abwasser zur Entsorgung stark vergrößern. Auch gibt es in der EU viele Labore, die eine große Anzahl Analysesysteme parallel laufen lassen. Gleichzeitig wird die Konzentration von NPE bzw. OPE im Abwasser über die Jahre durch die schrittweise Substitution immer weiter abnehmen. Letztlich kann der logistische Aufwand für die Sammlung und die Kosten für Transport und Entsorgung der Abwässer erheblich sein. Ganz zu schweigen von CO2-Emissionen, die durch den Transport und die Verbrennung von im Wesentlichen hochverdünnten wässrigen Lösungen verursacht werden.
Betroffene Antragsteller beklagen daher, dass durch diese Auflage unverhältnismäßig hohe Kosten für das Gesundheitssystem entstehen würden. Außerdem kann man sich fragen, warum der aufwendige Zulassungsantrag letztlich auf die kontrollierten Bedingungen hinauslaufen soll, die die Voraussetzungen für die Ausnahme von der Zulassung für die wissenschaftliche Forschung auch ohne Antrag erfüllen würden (siehe oben).
Andererseits wird die Sammlung und separate Entsorgung von Krankenhaus- und Laborabwässern auch aus anderen Gründen als notwendige Maßnahme diskutiert. Denn NP und OP sind noch nicht einmal die potentesten hormonaktiven Substanzen, die über diesen Weg in Gewässer gelangen können. Weitere Mikroschadstoffe wie Arzneimittel, gesundheitsschädliche Nachweisreagenzien, Mikroplastik oder andere persistente Stoffe können enthalten sein4.
Ob die Kommission in ihren Entscheidungen den Empfehlungen des RAC folgen wird, ist noch unklar. Sie ist anders als der RAC angehalten, die Verhältnismäßigkeit von Maßnahmen in ihren Entscheidungen zu berücksichtigen. Das Ablaufdatum ist wie gesagt der 4. Januar 2021. Beantragte Verwendungen, über die bis zu diesem Datum nicht entschieden wurde, dürfen weiter erfolgen, solange der Antrag nicht abgelehnt wurde. Wenn die Kommission die Auflagen aber in ihre Entscheidung übernimmt, wird den betroffenen Anwendern – Laboren und Krankenhäusern – möglicherweise nur eine kurze Frist gewährt, um sich auf die konsequente Sammlung und Entsorgung der Abwässer einzustellen.
Fußnoten
1 SVHC = Substances of very high concern nach REACH Artikel 59(1)
2 Der Stand aller eingereichten Anträge und die veröffentlichten Dokumente können auf der ECHA-Seite unter https://echa.europa.eu/de/applications-for-authorisation-previous-consultations abgerufen werden.
3 PNEC = Predicted no effect concentration
4 Siehe z. B. https://www.umweltbundesamt.de/
publikationen/massnahmen-zur-verminderung-des-eintrages-von‑0
Autorin: Kerstin Heitmann
Compliance for Chemicals
REACH Artikel 57 Nr. (f)
Stoffe – wie etwa solche mit endokrinen Eigenschaften oder solche mit persistenten, bioakkumulierbaren und toxischen Eigenschaften oder sehr persistenten und sehr bioakkumulierbaren Eigenschaften, die die Kriterien der Buchstaben d oder e nicht erfüllen –, die nach wissenschaftlichen Erkenntnissen wahrscheinlich schwerwiegende Wirkungen auf die menschliche Gesundheit oder auf die Umwelt haben, die ebenso besorgniserregend sind wie diejenigen anderer in den Buchstaben a bis e aufgeführter Stoffe, und die im Einzelfall gemäß dem Verfahren des Artikels 59 ermittelt werden.
ECHA Q&A ID 1442
Does the exemption for the use of Annex XIV substances in scientific research and development (SRD) under Article 56(3) of REACH also apply to analytical activities using in vitro diagnostic (IVD) medical devices (as defined in Directive 98/79/EC) at a laboratory scale?
Yes. The use of an Annex XIV substance when it is required, on its own or in a mixture, as part of an in vitro diagnostic (IVD) method (e.g. in a reagent, calibrator, control material or kit) is considered as scientific research and development and is therefore exempted from authorisation requirements if this activity is carried out under controlled conditions and in a volume not exceeding one tonne per year per legal entity. (https://echa.europa.eu/de/support/qas-support/browse/-/qa/70Qx/view/scope/REACH/Authorisation)